El estudio clínico internacional “Solidaridad”, impulsado desde marzo pasado por la Organización Mundial de la Salud (OMS) para conocer la efectividad de los fármacos remdesivir, hidroxicloroquina, ritonavir/lopinavir e interferón contra la enfermedad Covid-19, todavía no está en marcha en Panamá.
La investigación, diseñada para generar datos sólidos y demostrar qué tratamientos son los más eficaces contra la enfermedad durante estos meses, ha tenido vaivenes, debido al uso de fármacos, como la hidroxicloroquina y lopinavir/ritonavir.
En Panamá, la exministra de Salud Rosario Turner anunció en conferencia de prensa, a finales de marzo pasado, que el país formaría parte de esta investigación, diseñada para aplicar cuatro protocolos de medicamentos a los pacientes que padecen la Covid-19.
El objetivo del estudio es evaluar el efecto de los medicamentos en tres importantes desenlaces en pacientes con la enfermedad: mortalidad, necesidad de respiración asistida y duración de la hospitalización.
Turner atribuyó el ingreso de Panamá a la investigación al manejo transparente de la información sobre el nuevo coronavirus SARS CoV-2 con la población.
Los primeros resultados de esta investigación ya fueron divulgados en un preimpreso publicado el pasado 15 de octubre en el medRxiv, pero Panamá no aparece en la lista de los que brindaron resultados preliminares.

Ana Belén Araúz, presidenta de la Sociedad de Enfermedades Infecciosas de Panamá y una de las científicas principales del estudio en el país, explicó que el protocolo de investigación ya fue aprobado por el Comité Nacional de Bioética de la Investigación (CNBI), pero al ser un estudio adaptativo ha tenido múltiples cambios en los brazos del tratamiento, por lo que aún no ha comenzado.
Subrayó que están en espera de la enmienda más reciente que realizó la OMS al estudio, para obtener los medicamentos.
A la fecha, Panamá no ha iniciado el reclutamiento de pacientes, especificó la infectóloga.
Además, Araúz manifestó que el número de pacientes va a depender de cómo se comporte la pandemia en Panamá.
Proceso e CNBI
Este medio consultó en el CNBI –ente adscrito al despacho superior del Ministerio de Salud (Minsa) y creado mediante Decreto Ejecutivo No. 1843 de diciembre de 2014– y allí se informó que el estudio fue aprobado el pasado 8 de septiembre.
En la página web del CNBI se detalla que el protocolo de la investigación, titulado “Un ensayo aleatorizado internacional para evaluar tratamientos no licenciados para COVID-19 en pacientes hospitalizados que reciben el tratamiento convencional para Covid que se ofrece en cada hospital”, ingresó el pasado 7 de mayo.
Sin embargo, el protocolo de investigación debe ser revisado por los miembros del CNBI cada vez que se realizan cambios en el estudio, y cuando surgen preguntas o recomendaciones debe ser enviado al investigador principal para posteriormente volver a revisar la documentación.
El CNBI verifica que todo estudio tenga validez científica, validez social y que cumpla con los estándares éticos, según el artículo 38 de la Ley 84 de mayo 2019 y la Pauta 1 del Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS 2016).
Argentina Ying, presidenta del CNBI, explicó que se evalúa la solidez científica del estudio, de acuerdo con su diseño metodológico y la calidad de la información que generará.
Asimismo, se evalúa su pertinencia o la importancia de la información que producirá, y cómo garantizará que se respeten los derechos y la dignidad de los participantes, revisando que los riesgos no superen los beneficios y que se respete la voluntariedad del participante, entre otros aspectos, detalló Ying.
Cambios en el estudio
Las modificaciones en el brazo terapéutico que plantea la científica Araúz se encuentran detallados en la página web de la OMS, en la que se indica que el 4 de julio pasado el organismo aceptó la recomendación del grupo directivo internacional del ensayo Solidaridad de interrumpir los grupos de tratamiento de la Covid-19 con hidroxicloroquina y lopinavir/ritonavir.
El grupo directivo internacional formuló esta recomendación, tras comparar los resultados provisionales obtenidos en este ensayo entre el grupo de tratamiento con hidroxicloroquina y el grupo de tratamiento con lopinavir/ritonavir con el tratamiento de referencia, así como los datos procedentes de todos los ensayos presentados en la Cumbre de Investigación e Innovación sobre la Covid-19 organizada por la OMS los días 1 y 2 de julio.
El infectólogo Javier Nieto sostuvo que cada vez que ocurren enmiendas a los brazos terapéuticos se debe someter nuevamente el protocolo de investigación a evaluación al Comité Nacional de Bioética para su respectiva aprobación, y en esa parte administrativa el estudio se retrasó.
Añadió que ha sido una investigación muy inestable por el tema de la hidroxiclorquina, con el que se iniciaron las enmiendas en los fármacos a utilizar, y por el lopinavir/ritonavir. Además, la última decisión fue incluir anticuerpos monoclonales en el ensayo.
Datos preliminares
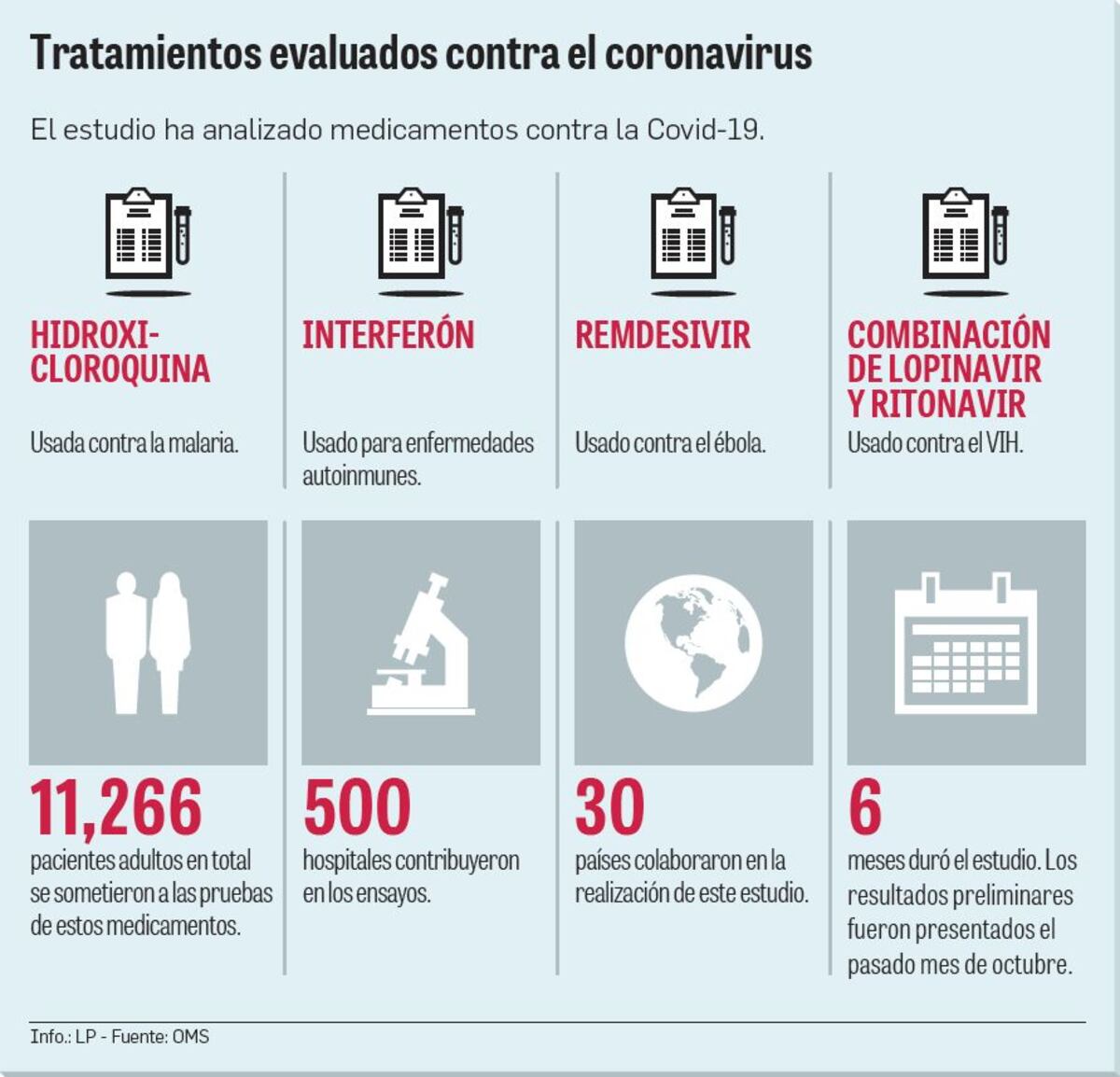
Los resultados preliminares del estudio Solidaridad, el ensayo de control terapéutico más grande, indican que el uso de remdesivir, hidroxicloroquina, lopinavir/ritonavir e interferón parecen tener poco o ningún efecto sobre la mortalidad a los 28 días o el curso de la Covid-19 entre pacientes hospitalizados.
Los ensayos, que incluyeron a 11 mil 266 pacientes de 400 hospitales de 30 países, analizaron los efectos de estos medicamentos. Si bien los datos del ensayo están en revisión para su publicación en una revista científica, fueron dados a conocer por la OMS de forma preliminar y se concluye que “los protocolos de remdesivir, hidroxicloroquina, lopinavir/ritonavir e interferón tienen poco o ningún efecto sobre los pacientes hospitalizados”.
Ivonne Torres-Atencio, directora del departamento de Farmacología de la Facultad de Medicina de la Universidad de Panamá, planteó que el estudio era adaptativo y se podían abandonar las drogas poco prometedoras y añadir otras, tal como sucedió con la hidroxicloroquina y el lopinavir, que fueron finalmente abandonados, pero otros, como los anticuerpos monoclonales, serán añadidos, ya que el estudio continúa en marcha.
“Lo que ha hecho la OMS es informar los resultados provisionales de mortalidad de los cuatro medicamentos originales del estudio”, expresó Torres-Atencio.


