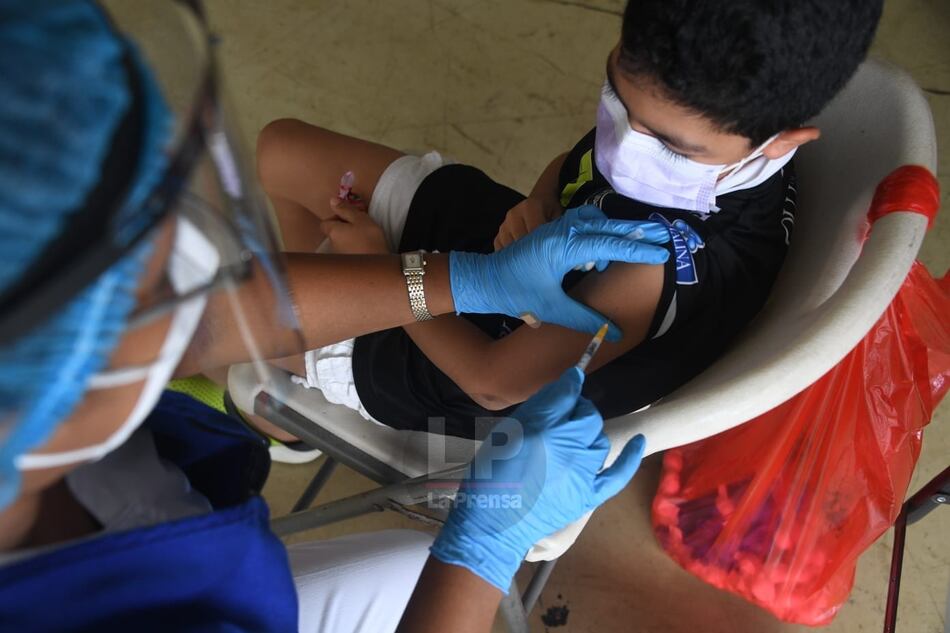
Pfizer y su socio BioNTech se preparan para pedir a las autoridades sanitarias de Estados Unidos (EU) que autoricen su vacuna anticovid en niños menores de 5 años, informaron ayer medios estadounidenses.
Si se aprueba, la vacuna de Pfizer/BioNTech sería la primera disponible en EU para este grupo de edad.
Según The Washington Post y The New York Times, la solicitud del grupo farmacéutico a la agencia reguladora de medicamentos (FDA) se refiere a un régimen de dos dosis y no de tres.
El anuncio ocurre cuando la ola de contagios por la variante ómicron disminuye en EU, pero los padres aún lidian con el cierre de escuelas y la preocupación por sus hijos no vacunados.
Las nuevas hospitalizaciones pediátricas por Covid-19 alcanzaron un récord en EU en diciembre.
En enero pasado, la FDA aprobó la vacuna anticovid de refuerzo, o tercera dosis, de Pfizer/BioNTech para niños de hasta 12 años.
Mientras buscan luz verde para que los niños menores de cinco años reciban dos dosis de la vacuna, Pfizer y BioNTech continuarán los estudios sobre un régimen de tres inyecciones, señaló The New York Times.
La FDA espera aprobar las vacunas para niños pequeños a fines de febrero. Los datos sobre un régimen de tres dosis no se enviarían hasta fines de marzo, agregó el diario.
Las compañías concluyeron a finales del año pasado que las dosis bajas de la vacuna brindaron protección en niños de hasta dos años, pero no en niños de 2 a 5 años, y anunciaron en diciembre que agregarían una tercera dosis a sus ensayos.